0 引言
瓦斯爆炸是威胁煤矿安全生产的主要灾害之一。煤矿一旦发生瓦斯爆炸事故,往往造成群死群伤。因此,瓦斯爆炸受到行业内学者的重点关注,在瓦斯燃炸极限[1]、压力特性[2]、火焰传播特性[3],以及初始压力[4]、初始温度[5]、障碍物[6-7]等环境因素对瓦斯爆炸特性的影响方面取得了大量研究成果。但针对瓦斯爆炸的研究大多以CH4与空气混合气体为研究对象,与井下气体环境有一定差异。
由于煤的氧化或热解作用,一般井下瓦斯爆炸事故并非单独的CH4爆炸,往往还存在CO,C2H4,H2等组分。特别是在煤的低温氧化、着火燃烧及热解过程中都会产生CO,使得CO在井下气体中的含量较高,对瓦斯爆炸产生一定影响。白刚等[8]研究了CO对瓦斯爆炸极限的影响,发现随着CO浓度升高,瓦斯爆炸极限范围变宽。邓军等[9]通过实验研究发现CO对CH4爆炸有一定的阻尼作用。S. A. El-sherif[10]研究发现添加少量的CO可有效提高CH4与空气混合气体的燃烧性能。然而目前CO对瓦斯爆炸的作用机理还不清晰。
本文在上述研究基础上,开展CO对CH4爆炸影响的实验和数值模拟研究,揭示CO对瓦斯爆炸反应的影响机理,可为井下瓦斯爆炸抑制剂、阻隔爆技术的开发提供基础数据。
1 瓦斯爆炸实验研究
瓦斯爆炸实验装置主要由20 L不锈钢球形爆炸罐、点火装置、数据采集系统、主控计算机等组成,如图1所示。将球形爆炸罐内空气抽出,使罐内形成负压。按一定配比注入CH4与CO,静置5 min后点火,点火能量为1 J。罐内混合气体被引燃的同时,数据采集系统记录并存储压力。实验在常温(22~25 ℃)常压(101 325 Pa)下进行。实验气体配比见表1。
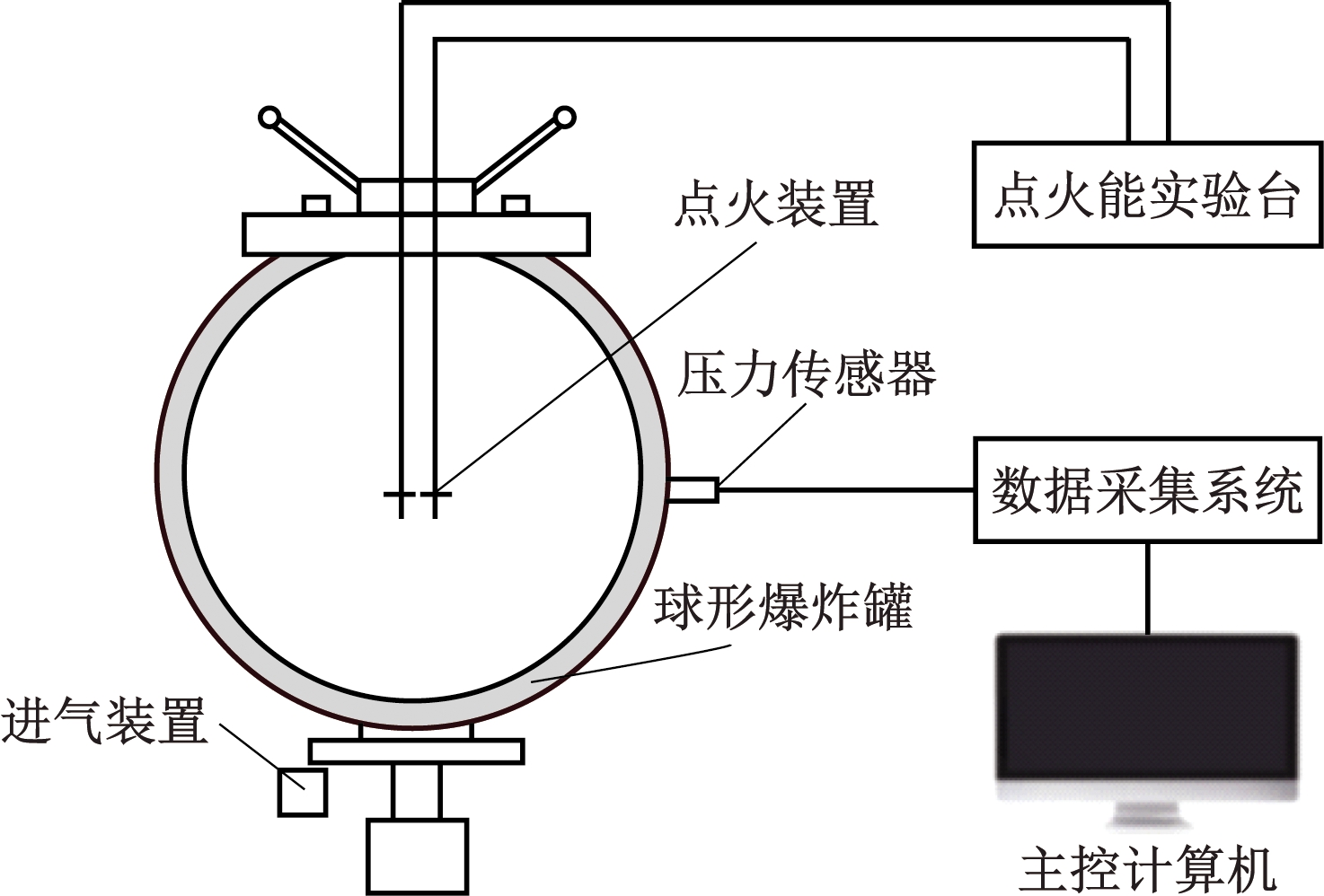
图1 瓦斯爆炸实验装置
Fig.1 Gas explosion experiment device
表1 实验气体配比
Table 1 Compounding ratios of experimental gas %
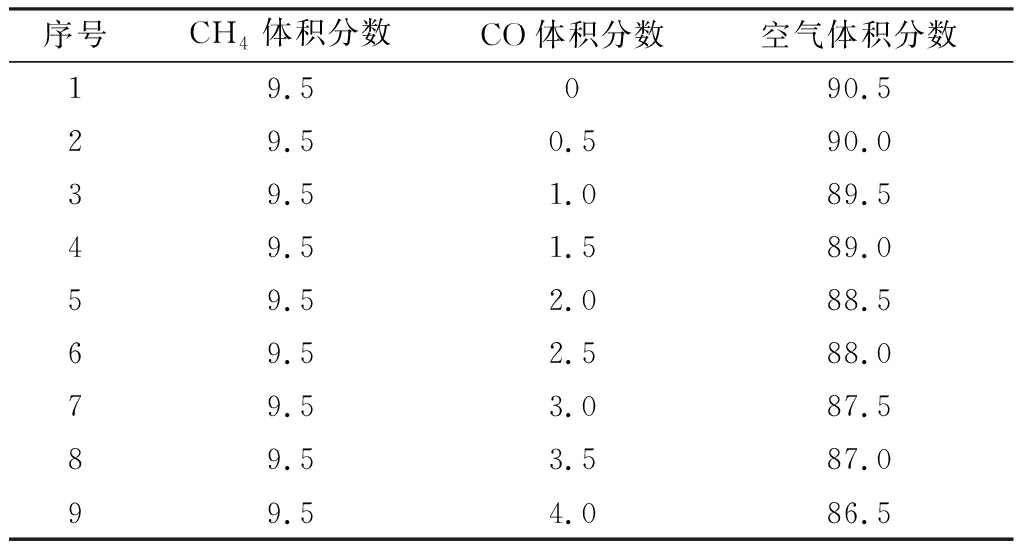
序号CH4体积分数CO体积分数空气体积分数19.5090.529.50.590.039.51.089.549.51.589.059.52.088.569.52.588.079.53.087.589.53.587.099.54.086.5
不同配比下混合气体最大爆炸压力如图2所示。可看出随着CO浓度增大,最大爆炸压力呈先增大后减小趋势,CO体积分数为2%时最大,为624.9 kPa。与未添加CO相比,CO体积分数小于3%时,混合气体最大爆炸压力存在一定程度提高,表明CO对9.5%CH4爆炸反应有一定促进作用;CO体积分数大于3%时,最大爆炸压力存在一定程度降低,此时CO对9.5%CH4爆炸反应产生一定的抑制作用。
2 瓦斯爆炸数值模拟
2.1 数值模拟原理
本文从基元反应的角度探索CO对瓦斯爆炸反应的影响机理。采用Chemkin-Pro数值模拟软件,选取封闭均质燃烧反应器模型和GRI-mech 3.0机理模拟计算瓦斯爆炸过程。GRI-mech 3.0机理包含53种物质和325个基元反应,能够很好地求解和计算CH4燃烧机理,且包含了CO所有燃烧反应步骤,是应用最广泛的化学反应机理之一[11-13]。GRI-mech 3.0机理主要包括以下控制方程。
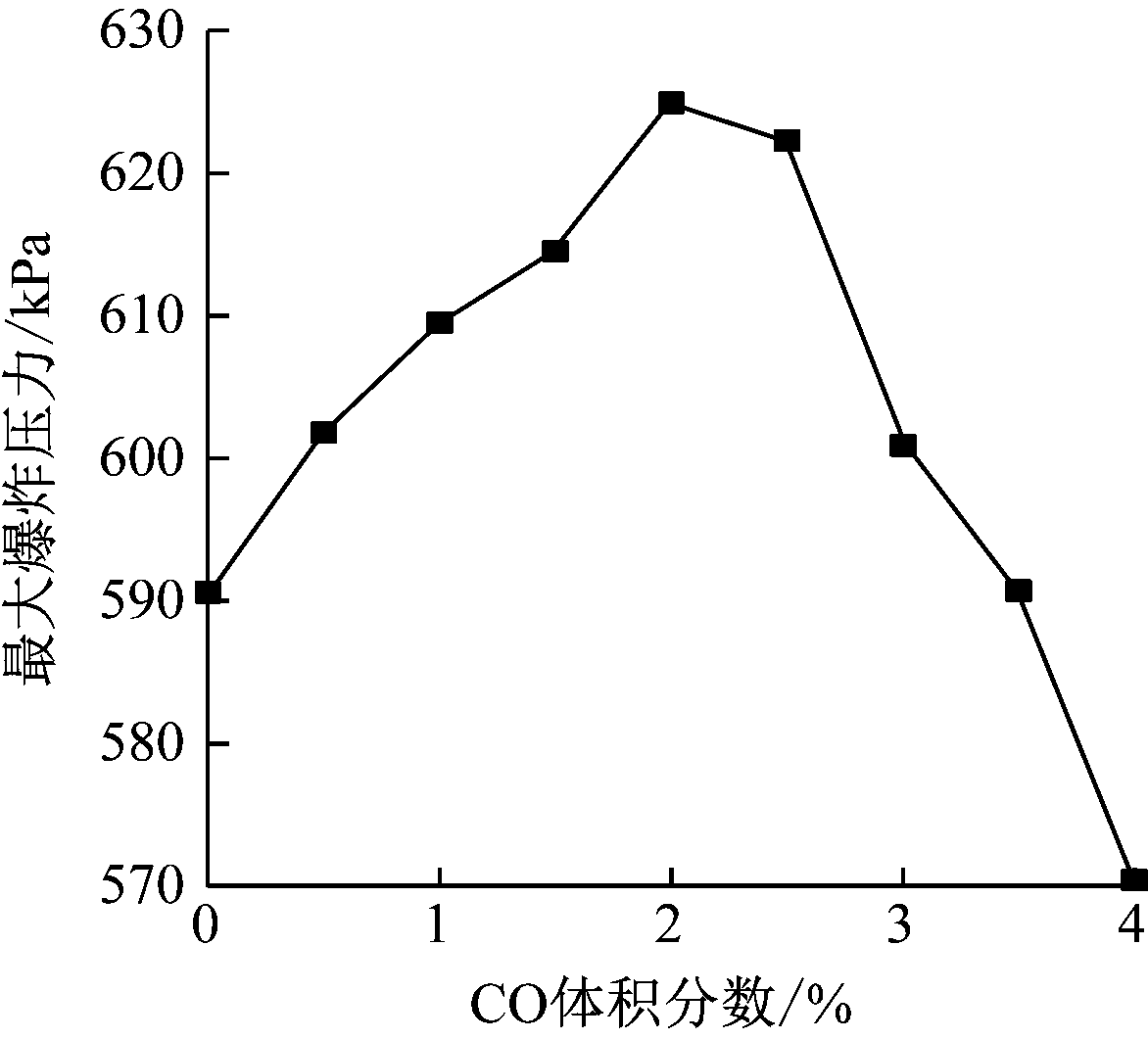
图2 混合气体最大爆炸压力
Fig.2 The maximum explosion pressure of gas mixture
组分方程:
(1)
式中:Yi为第i(i=1,2,…,k,k为混合气体组分总数)种组分的质量分数,%;t为时间,s;V为混合气体的比热容,m3/kg;wi为第i种组分的净生成速率,mol/(cm3·s);Mi为第i种组分的摩尔质量,g/mol。
(2)
(3)
式中:N为爆炸反应总步数;vim为第m步反应中第i种组分的计量系数;Km为第m步反应的正反应速率常数;Xi为第i种组分的物质的量浓度,mol/cm3;Am为第m步反应的指前因子,s-1;T 为温度,K;bm为第m步反应的温度指数;Em为第m步反应的活化能,J/mol;R为混合气体的气体常数,J/(mol·K)。
能量方程:
(4)
式中:c为定容比热容,J/(kg·K);ei为第i种组分的内能,J。
2.2 数值模拟分析
2.2.1 温度敏感性分析
瓦斯爆炸反应在极短的时间内即可完成,因此在Chemkin-Pro软件的数值模型中将爆炸反应看作在一个完全绝热封闭环境内完成。从化学动力学的角度看,温度既是爆炸强度的体现,也是引发和维持链式反应的必要条件。实验中难以测量瞬态温度,而温度与超压这2个爆炸特征参数高度相关,温度升高必然导致压力增大,且爆炸超压也是产生破坏的主要因素。因此,在实验中仅测试了最大爆炸超压(即最大爆炸压力),而在数值模拟中重点研究CO对爆炸反应温度的影响。温度敏感性前10的基元反应见表2。
表2 温度敏感性前10的基元反应
Table 2 Elementary reactions with top 10 temperature sensitivity
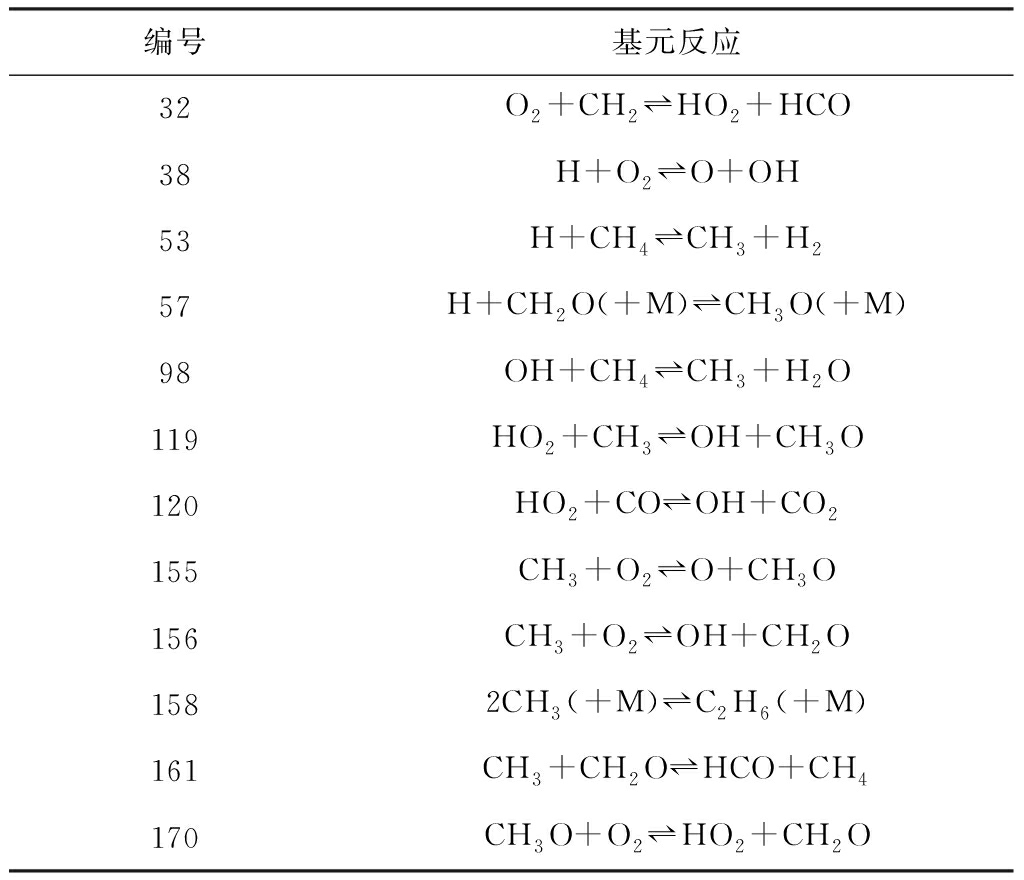
编号基元反应32O2+CH2⇌HO2+HCO38H+O2⇌O+OH53H+CH4⇌CH3+H257H+CH2O(+M)⇌CH3O(+M)98OH+CH4⇌CH3+H2O119HO2+CH3⇌OH+CH3O120HO2+CO⇌OH+CO2155CH3+O2⇌O+CH3O156CH3+O2⇌OH+CH2O1582CH3(+M)⇌C2H6(+M)161CH3+CH2O⇌HCO+CH4170CH3O+O2⇌HO2+CH2O
对9.5%CH4和9.5%CH4添加2%CO的混合气体在1 300 K时的各基元反应温度敏感性进行数值模拟,结果如图3所示。可看出:2种情况下温度敏感性前5的基元反应一致,包括正反应155,156,38号,以及负反应158,53号;与9.5%CH4爆炸反应相比,添加2%CO后,除57号基元反应被替换为98号外,其余基元反应敏感性排序无变化。
为分析CO对瓦斯爆炸基元反应的影响,对不同CO浓度下瓦斯爆炸温度敏感性系数前10进行归一化处理,结果如图4所示。可看出随着CO浓度增大,120号基元反应HO2+CO OH+CO2 逐渐增强,在CO体积分数为2%时进入温度敏感性前10,同时170号基元反应CH3O+O2
OH+CO2 逐渐增强,在CO体积分数为2%时进入温度敏感性前10,同时170号基元反应CH3O+O2 HO2+CH2O逐渐减弱,直至退出温度敏感性前10。导致该现象的原因:CO促进了120号基元反应,且大部分CO被120号基元反应消耗;随着CO浓度增大,反应体系的贫氧程度逐渐加剧,减弱了170号基元反应。此外,添加CO后,57号基元反应H+CH2O(+M)
HO2+CH2O逐渐减弱,直至退出温度敏感性前10。导致该现象的原因:CO促进了120号基元反应,且大部分CO被120号基元反应消耗;随着CO浓度增大,反应体系的贫氧程度逐渐加剧,减弱了170号基元反应。此外,添加CO后,57号基元反应H+CH2O(+M) CH3O(+M)被98号基元反应OH+CH4
CH3O(+M)被98号基元反应OH+CH4 CH3+H2O替代,证明CO促进了CH4的脱氢反应。
CH3+H2O替代,证明CO促进了CH4的脱氢反应。
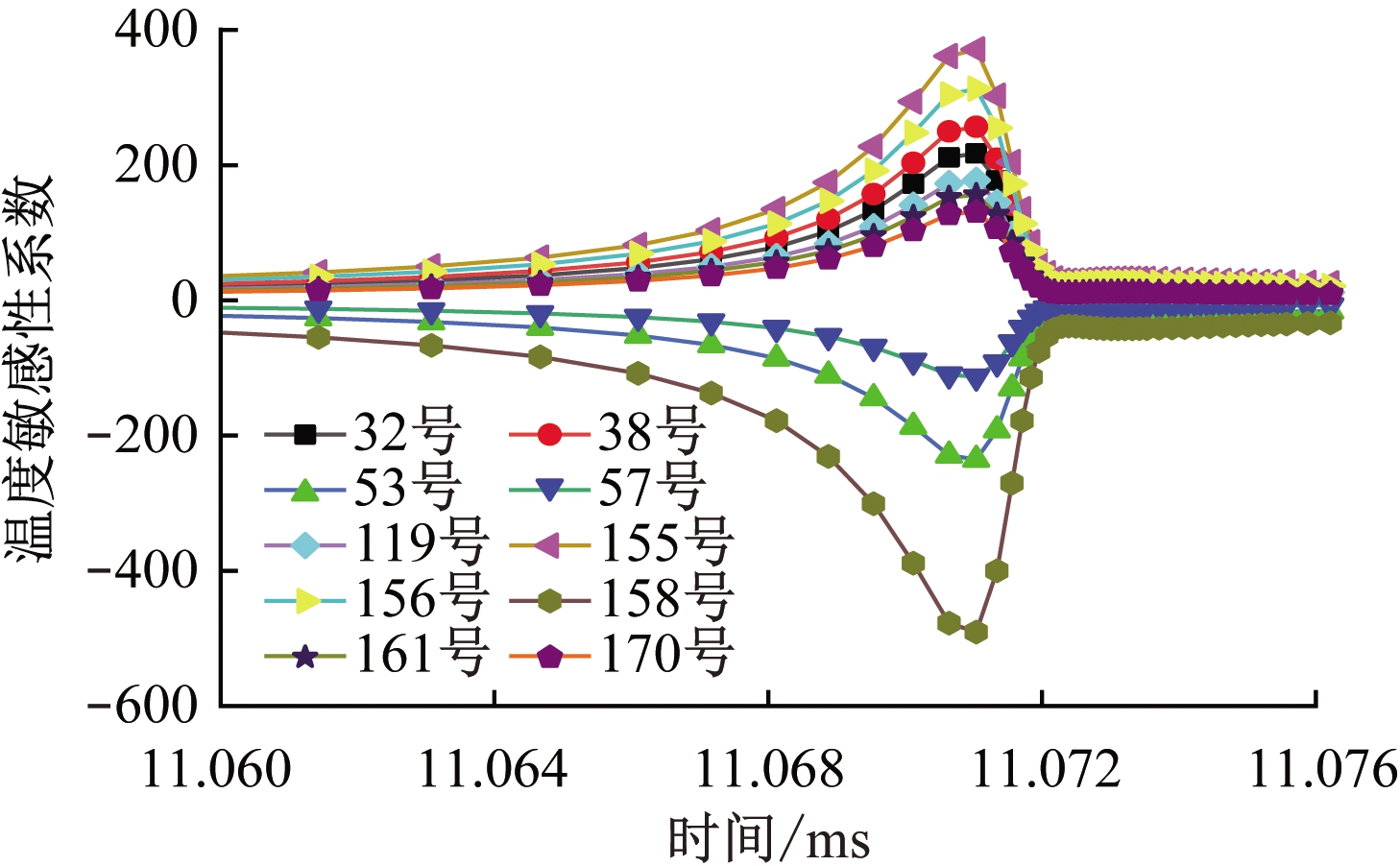
(a) 9.5%CH4

(b) 9.5%CH4+2%CO
图3 温度敏感性数值模拟结果
Fig.3 Numerical simulation results of temperature sensitivity
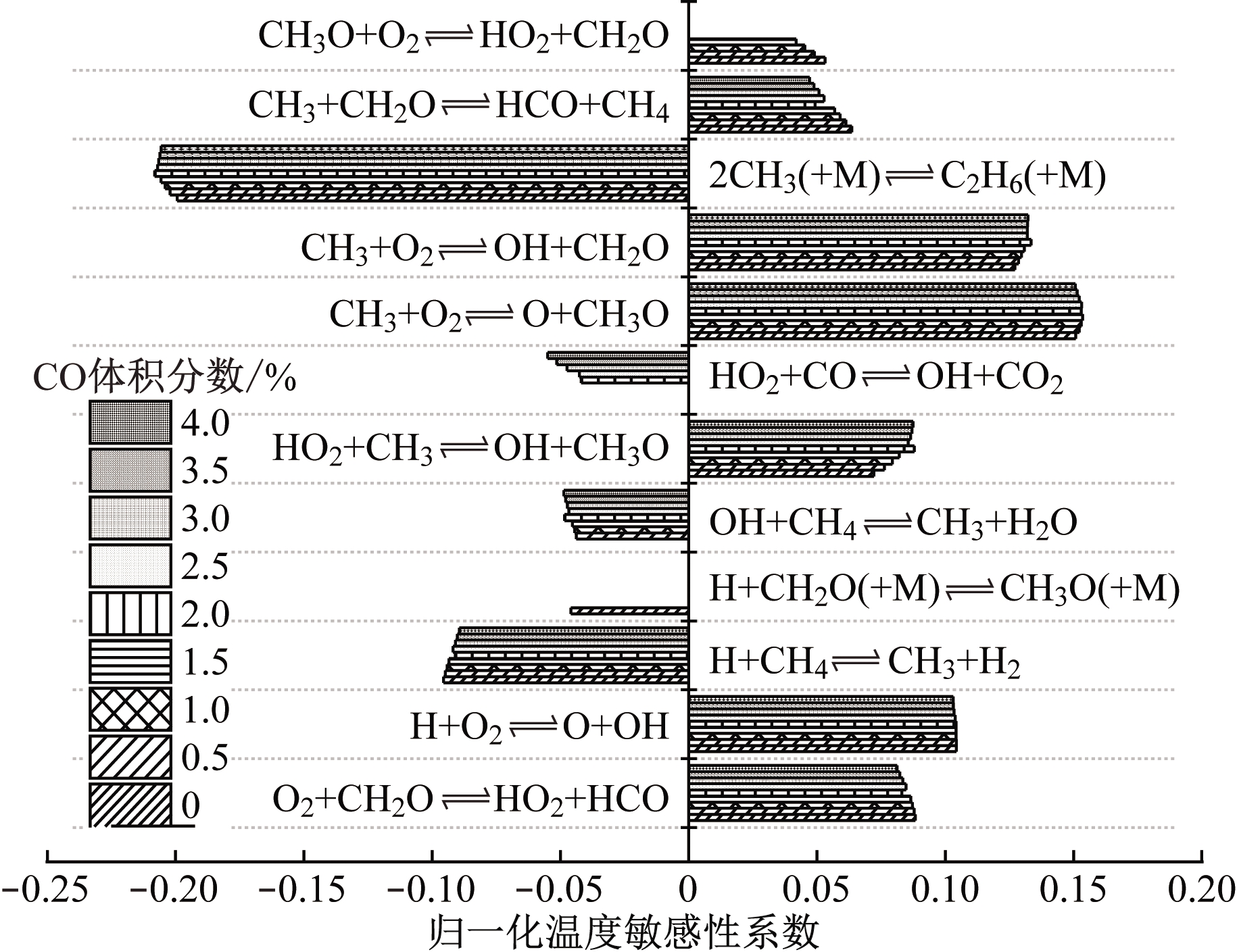
图4 不同CO浓度下基元反应的温度 敏感性系数归一化结果
Fig.4 Normalized results of temperature sensitivity coefficients of elementary reactions under different CO concentrations
从图4还可看出,不同CO浓度下基元反应的温度敏感性系数不同。直接对比温度敏感性系数很难看出基元反应对CO浓度变化的响应程度。因此,引入温度敏感性变化系数。以9.5% CH4爆炸各基元反应的温度敏感性系数S0为参考,计算不同CO浓度下瓦斯爆炸基元反应的温度敏感性变化系数:
(5)
式中Sn为添加CO后基元反应n(n为基元反应编号)的温度敏感性系数。
定义添加CO后退出温度敏感性前10的基元反应的温度敏感性变化系数为-1,添加CO后新进入温度敏感性前10的基元反应的温度敏感性变化系数为1。ΔS >0表示该基元反应的温度敏感性系数与CO浓度正相关,反之为负相关。不同CO浓度下基元反应的温度敏感性变化系数如图5所示。温度敏感性系数大于0的基元反应促进温度升高,而温度敏感性系数小于0的基元反应抑制温度升高。

图5 不同CO浓度下基元反应的温度敏感性变化系数
Fig.5 Temperature sensitivity variation coefficients of elementary reactions under different CO concentrations
从图5可看出:ΔS >0的基元反应主要有120号HO2+CO OH+CO2、 98号OH+CH4
OH+CO2、 98号OH+CH4 CH3+H2O、119号HO2+CH3
CH3+H2O、119号HO2+CH3 OH+CH3O,说明随着CO浓度增大,120,98,119号基元反应增强;ΔS <0的基元反应主要有57号H+CH2O(+M)
OH+CH3O,说明随着CO浓度增大,120,98,119号基元反应增强;ΔS <0的基元反应主要有57号H+CH2O(+M) CH3O(+M)、170号CH3O+O2
CH3O(+M)、170号CH3O+O2 HO2+CH2O,说明随着CO浓度增大,57,170号基元反应减弱;120,98,57号基元反应的温度敏感性系数为负,119,170号基元反应的温度敏感性系数为正。
HO2+CH2O,说明随着CO浓度增大,57,170号基元反应减弱;120,98,57号基元反应的温度敏感性系数为负,119,170号基元反应的温度敏感性系数为正。
9.5%为CH4与空气混合气体爆炸反应的理论化学计量体积分数。由于CH4未完全反应、CH4分子分布不均等原因,实际中CH4体积分数为10%时爆炸压力最大[14]。9.5%CH4与空气混合气体处于贫燃料状态,因此添加一定量(体积分数小于3%)的CO后,体现为爆炸压力增大。随着CO浓度增大,促进温度升高的主要基元反应被抑制,抑制温度升高的主要基元反应被促进,宏观体现为随着CO浓度增大,爆炸反应体系温度降低,最大爆炸压力增大。
2.2.2 关键自由基分析
点火延迟时间是反映可燃气体燃爆特性的重要参数,自由基·OH浓度反映了瓦斯爆炸反应的强弱[15]。本文将从点火至达到·OH峰值浓度所耗费的时间定义为点火延迟时间。不同CO浓度下混合气体点火延迟时间如图6所示。
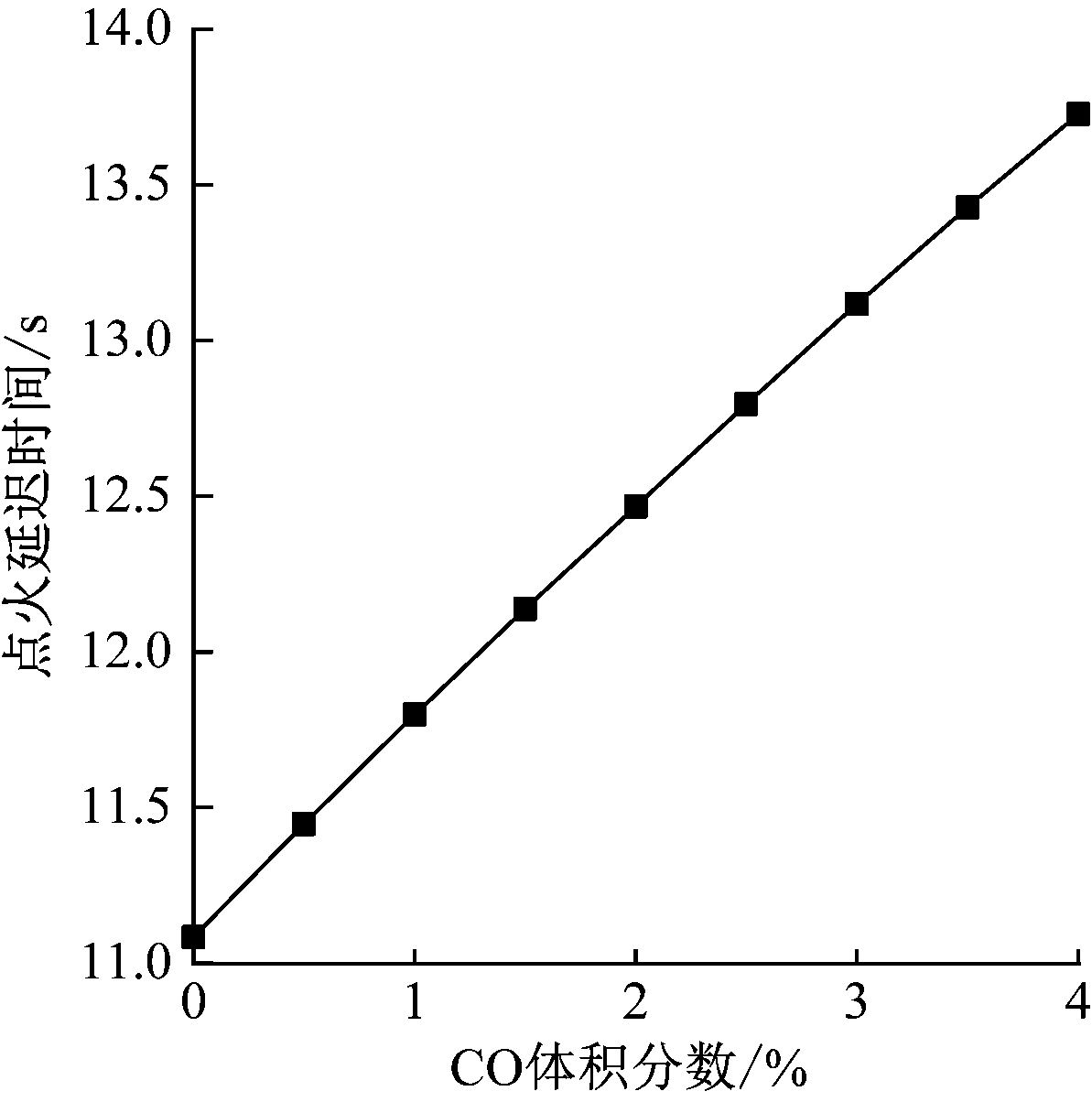
图6 混合气体点火延迟时间
Fig.6 Ignition delay time of gas mixture
由图6可看出,添加CO后,CH4爆炸反应的点火延迟时间增大,且增幅随CO浓度增大而增大,从而降低了CH4爆炸反应速率。
自由基·OH,·O,·H,·HCO在链引发阶段和支链反应中都起关键作用,是决定反应剧烈程度的重要因素[16]。采用GRI-mech 3.0机理计算自由基·OH,·O,·H,·HCO物质的量浓度,结果如图7所示。可看出添加CO后,4种自由基峰值物质的量浓度的出现时间均有所延迟,且随着CO浓度增大,延迟幅度增大。这在一定程度上验证了点火延迟时间的分析结果。另外,添加CO后,自由基·OH,·O的峰值物质的量浓度减小,自由基·H的峰值物质的量浓度增大,在一定程度上验证了温度敏感性分析结果,即添加CO加剧了CH4脱氢反应,进而增大了·H自由基浓度。
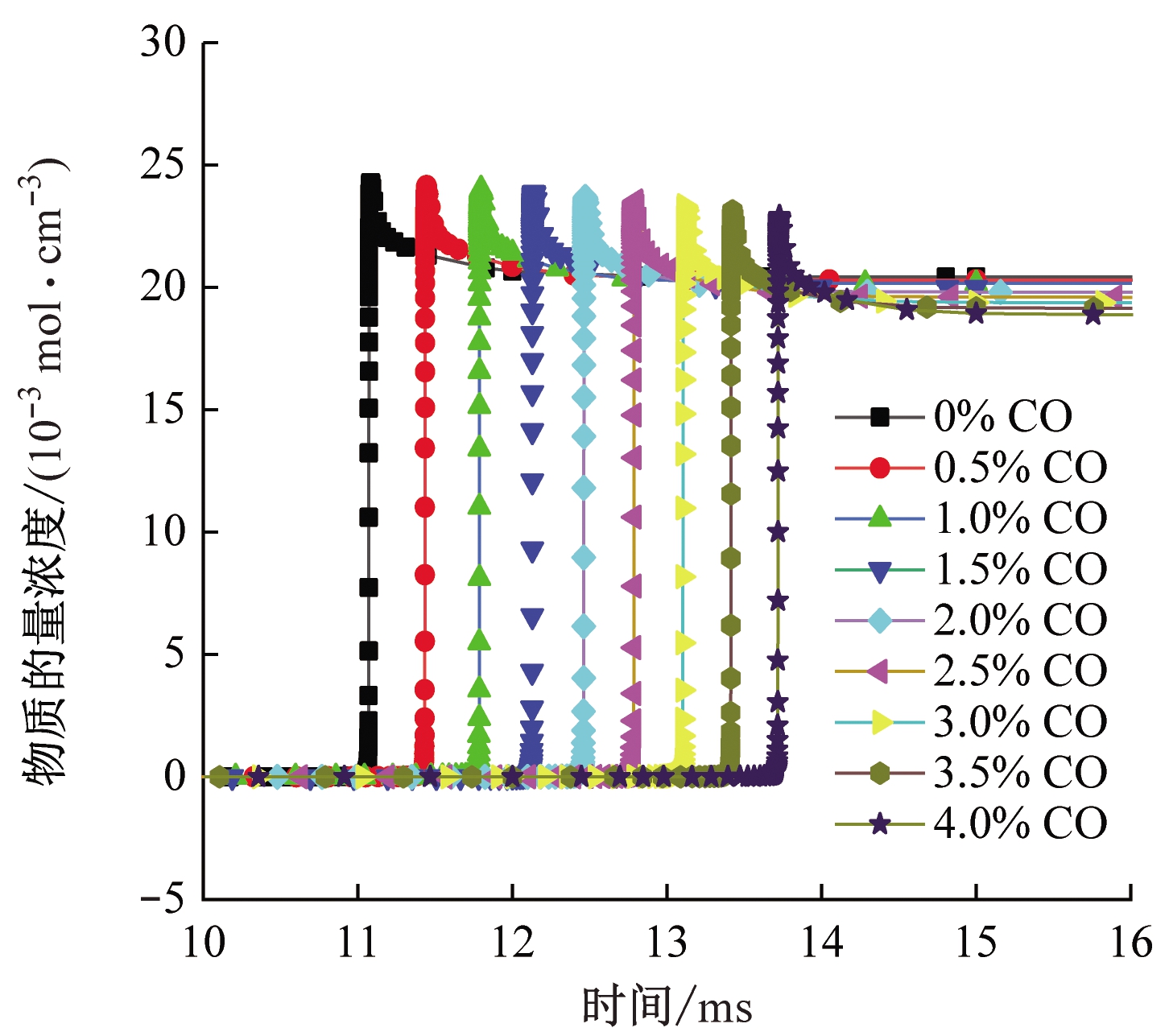
(a) ·OH
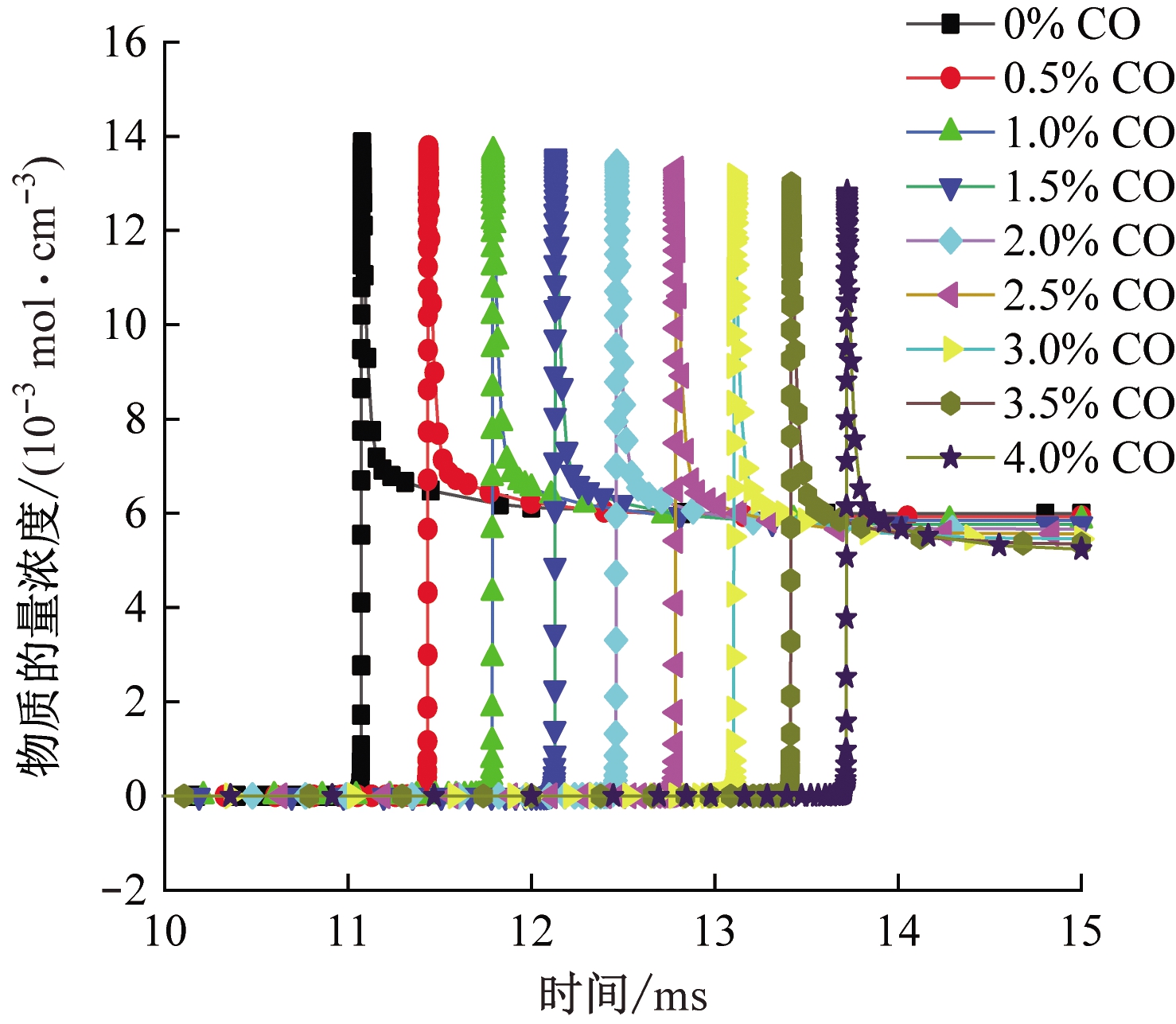
(b) ·O
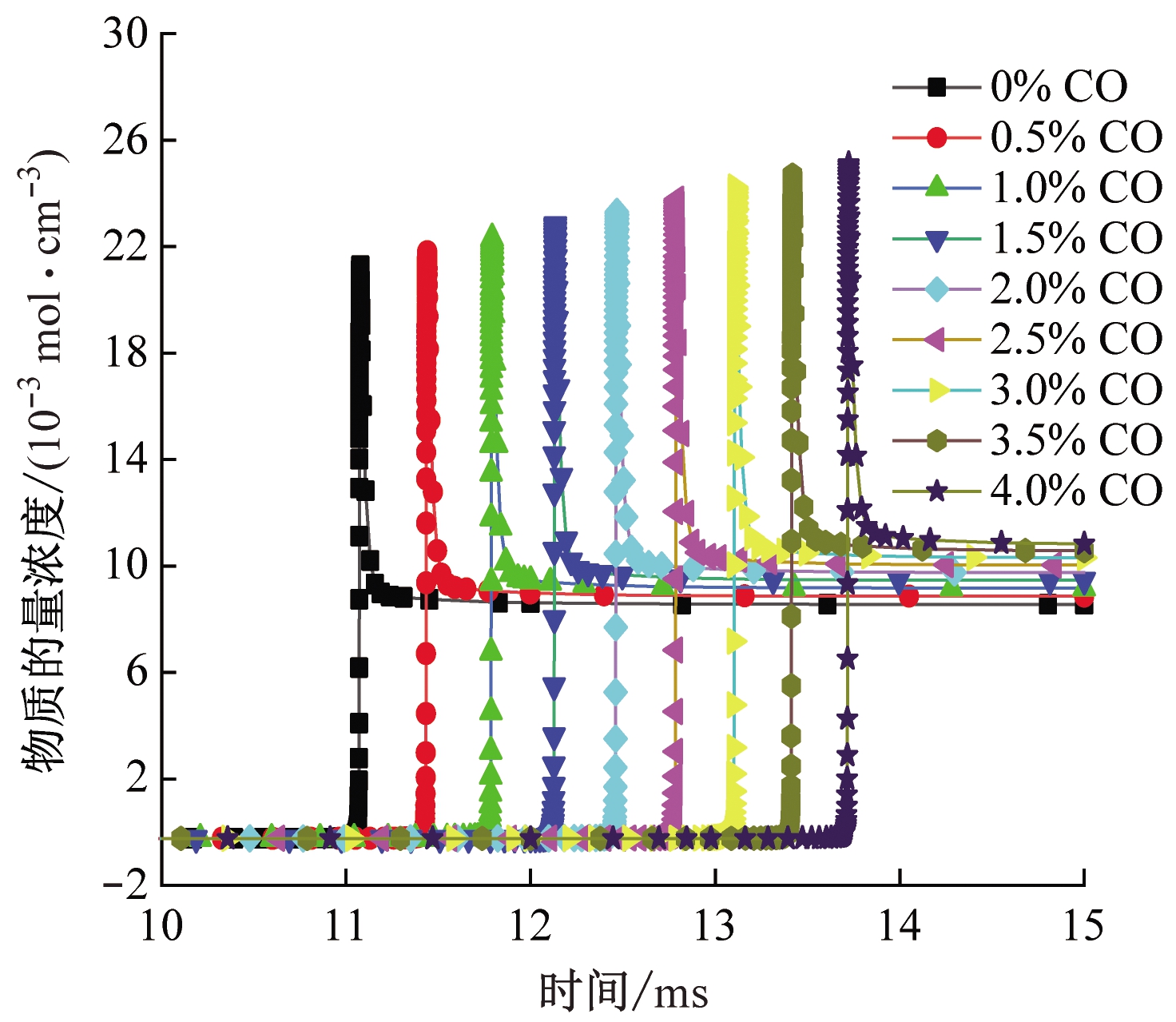
(c) ·H
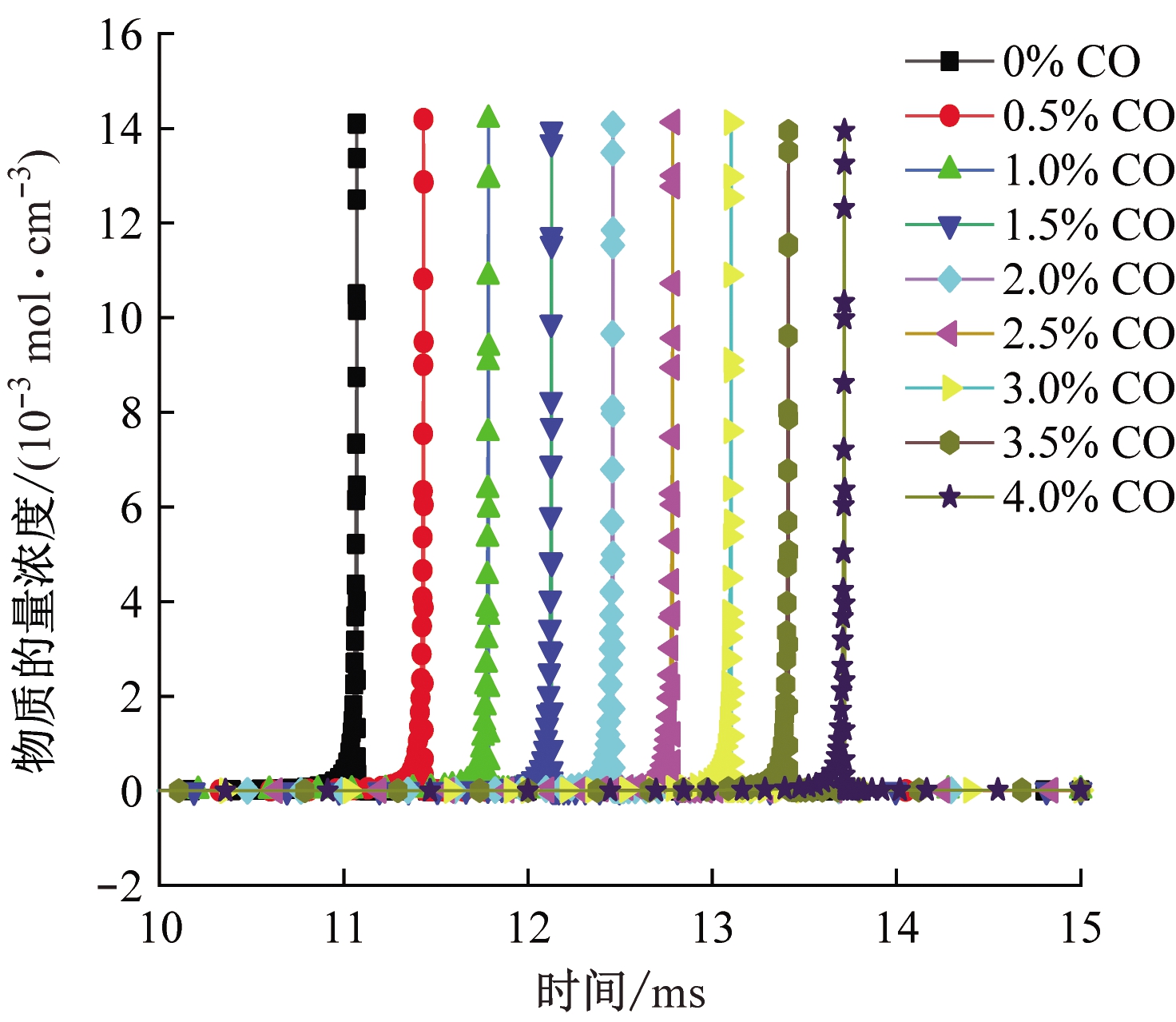
(d) ·HCO
图7 关键自由基浓度变化
Fig.7 Concentration variation of key free radicals
3 结论
(1) 通过20 L球形爆炸罐测试了不同配比CO,CH4与空气混合气体的最大爆炸压力,研究了CO对瓦斯爆炸强度的影响规律。当CH4体积分数为9.5%时,随着添加的CO浓度增大,混合气体最大爆炸压力呈先增大后减小趋势,CO体积分数为2%时最大,为624.9 kPa。
(2) 在Chemkin-Pro数值模拟软件中利用GRI-mech 3.0机理对CO,CH4与空气混合气体爆炸反应进行了温度敏感性和关键自由基分析,从化学动力学角度分析了CO对瓦斯爆炸反应的影响机理。在9.5%CH4,CO与空气混合气体爆炸反应体系中, CO既充当燃料与O2反应,也参与CH4与O2的链式反应。添加少量CO时,CO主要充当燃料,使反应体系中燃料浓度接近化学计量值,促使最大爆炸压力增大;随着CO浓度增大,反应体系出现贫氧状态,且由于CO对CH4链式反应产生影响,使得最大爆炸压力减小。
(3) 添加CO促进了阻碍温度升高的98,120号基元反应,抑制了促进温度升高的57,170号基元反应。同时,CO对自由基峰值物质的量浓度出现时间有一定的延迟效应,因此添加CO后,瓦斯爆炸反应的点火延迟时间增大。
[1] CUI Gan,YANG Chao,LI Zili,et al.Experimental study and theoretical calculation of flammability limits of methane/air mixture at elevated temperatures and pressures[J].Journal of Loss Prevention in the Process Industries,2016,41:252-258.
[2] MITU M,GIURCAN V,RAZUS D,et al.Propagation indices of methane-air explosions in closed vessels[J]. Journal of Loss Prevention in the Process Industries,2017,47:110-119.
[3] GUO Shilong,WANG Jinhua,ZHANG Weijie,et al. Investigation on bluff-body and swirl stabilized flames near lean blowoff with PIV/PLIF measurements and LES modelling[J].Applied Thermal Engineering,2019,160:114021.
[4] CUI Gan,LI Zili,YANG Chao.Experimental study of flammability limits of methane/air mixtures at low temperatures and elevated pressures[J].Fuel,2016,181:1074-1080.
[5] HU Erjiang,HUANG Zuohua,HE Jiajia,et al.Experimental and numerical study on lean premixed methane-hydrogen-air flames at elevated pressures and temperatures[J].International Journal of Hydrogen Energy,2009,34(16):6951-6960.
[6] ZHOU Shangyong,GAO Jiancun,LUO Zhenmin,et al.Effects of mesh aluminium alloy and aluminium velvet on the explosion of H2/air, CH4/air and C2H2/air mixtures[J]. International Journal of Hydrogen Energy,2021,46(28):14871-14880.
[7] 王磊.球形障碍物对瓦斯爆燃火焰影响试验研究[J].中国安全科学学报,2021,31(3):54-59.
WANG Lei.Experimental study on effect of spherical obstacle on gas deflagration flame[J].China Safety Science Journal,2021,31(3):54-59.
[8] 白刚,周西华,宋东平.温度与CO气体耦合作用对瓦斯爆炸界限影响实验[J].高压物理学报,2019,33(4):189-196.
BAI Gang,ZHOU Xihua,SONG Dongping.Experimental study on the coupling influence of temperature and CO concentration on CH4 explosion limit[J].Chinese Journal of High Pressure Physics,2019,33(4):189-196.
[9] 邓军,吴晓春,程超.CH4,CO,C2H4多元可燃气体爆炸的实验研究[J].煤矿现代化,2007(5):63-65.
DENG Jun,WU Xiaochun,CHENG Chao.Experimental study on explosion of multicomponent combustibility gases containing CH4,CO,C2H4[J].Coal Mine Modernization,2007(5):63-65.
[10] EL-SHERIF S A. Control of emissions by gaseous additives in methane-air and carbon monoxide-air flames[J].Fuel,2000,79:567-575.
[11] HU Erjiang,LI Xiaotian,MENG Xin,et al. Laminar flame speeds and ignition delay times of methane-air mixtures at elevated temperatures and pressures[J].Fuel,2015,158:1-10.
[12] SCHWER D A, LU Pisi, GREEN W H.An adaptive chemistry approach to modeling complex kinetics in reacting flows[J].Combustion and Flame,2003,133(4):451-465.
[13] 乔瑜,徐明厚,姚洪.基于敏感性分析的甲烷反应机理优化简化[J].华中科技大学学报(自然科学版),2007,35(5):85-87.
QIAO Yu,XU Minghou,YAO Hong.Optimally-reduced kinetic models for GRI-mech 3.0 combustion mechanism based on sensitivity analysis[J].Journal of Huazhong University of Science and Technology(Nature Science Edition),2007,35(5):85-87.
[14] 郝健池.矿井可燃性气体爆炸特性研究[J].煤炭技术,2015,34(10):152-154.
HAO Jianchi.Research on combustible gas explosion characteristic[J].Coal Technology,2015,34(10):152-154.
[15] YAMAMOTO K,OZEKI M,HAYASHI N, et al. Burning velocity and OH concentration in premixed combustion[J]. Proceedings of the Combustion Institute,2009,32(1):1227-1235.
[16] XIAO Peng,LEE C F,WU Han,et al.Impacts of hydrogen-addition on methanol-air laminar burning coupled with pressures variation effects[J].Energy,2019,187:115997.
